ZB-18a Zespół Materiałów Magnetycznych
Kierownik: prof. dr hab. Alina Bieńko

Osiągnięcia badawcze
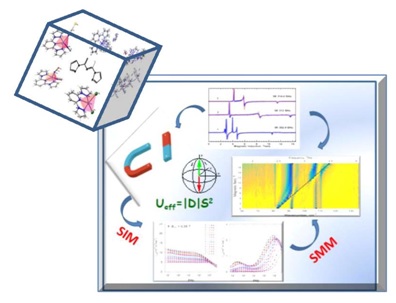
Wykrycie i charakterystyka teoretyczna dynamiki procesów powolnej relaksacji w serii pięcio-i sześciokoordynacyjnych kompleksów Co(II) wykazujących wysokie wartości bariery odwracalności spinu w połączeniu z długimi czasami relaksacji. Potwierdzenie dużej, dodatniej anizotropii w otrzymanych materiałach Co(II) (parametr D) spektroskopią HF EPR wysokich pól i wysokich częstości w połączeniu z metodą FIRMS. Określenie wpływu ligandów N-donorowych, halogenowych oraz pseudhalogenowych na wielkość anizotropii magnetycznej oraz ich roli w konstrukcji SMM lub SIM. Problematyka dostrajania właściwości magnetycznych związków poprzez modyfikacje ich struktury molekularnej i elektronowej została szczegółowo opisana w publikacjach: Inorganic Chemistry Frontiers, 2021, 8, 4356-4366; doi: 10.1039/d1qi00667c, Inorganic Chemistry Frontiers, 2020, 7, 2637-2650; doi: 10.1039/d0qi00257g; Inorganic Chemistry, 2018, 57, 12740-12755, doi: 10.1021/acs.inorgchem.8b01906
Linki do publikacji:
https://pubs.rsc.org/en/content/articlelanding/2021/QI/D1QI00667C
https://pubs.rsc.org/en/content/articlelanding/2020/QI/D0QI00257G
https://pubs.acs.org/doi/10.1021/acs.inorgchem.8b01906
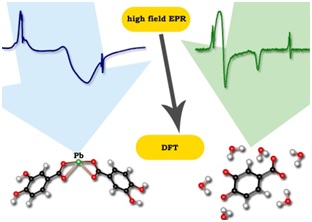
Widma EPR wysokich częstości oraz struktury obliczone w oparciu o metody DFT: kompleksu ołowiu(II) z rodnikiem o-semichinonowym otrzymanym z kwasu 3,4-dihydroxybenzoesowego (lewa strona) oraz wyjściowego rodnika w roztworze wodnym (prawa strona). Zarówno kompleks jak i wolny rodnik są modelami układów powstających w kwasach huminowych. Widma EPR wysokich częstości (416.00 GHz) zostały zarejestrowane na spektrometrze udostępnionym w NHMFL (http://www.magnet.fsu.edu/).
Szczegółowy opis badań został zawarty w publikacji: Physical Chemistry Chemical Physics, 2021, 23, 17408-17419; doi: 10.1039/d1cp01596f
Link do publikacji: https://pubs.rsc.org/en/content/articlelanding/2021/cp/d1cp01596f
Otrzymanie serii homo- i heterometalicznych kompleksów jonów metali z ligandami fosfinowymi będącymi pochodnymi antybiotyków fluorochinolonowych, peptydów oraz drugorzędowych amin o potencjalnych właściwościach przeciwnowotworowych (związki charakteryzowały się wyższymi wartościami indeksu terapeutycznego niż obecnie stosowane leki w chemioterapii). W znacznej większości udało ustalić się cytotoksyczny mechanizm działania otrzymanych związków, który znacznie różni się od mechanizmów obecnie stosowanych cytostatyków. Biodostępność i selektywność kompleksów o najlepszej aktywności została dodatkowo poprawiona poprzez zastosowanie różnego rodzaju nanoformulacji.

Więcej informacji w publikacjach:
Dalton Transactions, 2022, 51, 8605-8617; doi: (praca wyróżniona okładką)
Pharmaceuticals, 2022, 15, 169/1-169/22; doi: 10.3390/ph15020169
Scientific Reports, 2021, 11, 23943/1-23943/17; doi: 10.1038/s41598-021-03352-2
Inorganic Chemistry Frontiers, 2020, 7, 3386-3401; doi:10.1039/d0qi00538j
Linki do publikacji:
https://pubs.rsc.org/en/content/articlelanding/2022/dt/d2dt01055k
https://www.mdpi.com/1424-8247/15/2/169
https://www.nature.com/articles/s41598-021-03352-2
https://pubs.rsc.org/en/content/articlelanding/2020/qi/d0qi00538j
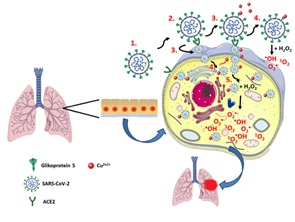
Zaproponowanie nowego, rodnikowozależnego mechanizmu uszkodzenia płuc w chorobie COVID-19. Potwierdzono, że jony Cu(II) są zdolne do tworzenia kompleksów z fragmentami glikoproteiny S wirusa SARS-CoV-2. Udowodniono produkcję różnego typu reaktywnych form tlenu (RFT) przez układy jon Cu(II)-fragment glikoproteiny S w obecności czynników utleniających i redukujących. Ustalono, że wytworzone RFT przyczyniają się do uszkodzenia DNA poprzez cięcie zarówno pojedynczej jak podwójnej nici DNA.